肺癌治疗中血小板减少的管理

摘要肺癌治疗过程中,血小板减少是影响疗效和安全性的重要并发症,与化疗、靶向治疗及免疫治疗密切相关。本文从病理机制、风险评估、分层管理和新兴治疗策略等方面综述现有循证依据,为临床实践提供参考。
引言
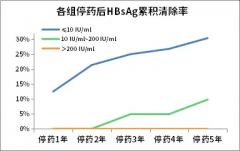
肺癌是我国发病率和死亡率最高的恶性肿瘤,2020年全球新发病例达220万例[1]。随着靶向治疗和免疫治疗的普及,患者生存期显著延长,但治疗相关血液学毒性日益受到关注。其中血小板减少(血小板计数<100×10?/L)发生率达15%-40%[2],严重者可导致出血事件或治疗中断。本文系统分析肺癌治疗中血小板减少的管理策略。
病因与发生机制
1. 化疗相关性血小板减少
含铂双药方案(如卡铂/紫杉醇)通过抑制骨髓巨核细胞分化导致血小板减少,发生率为25%-35%[3]。培美曲塞等抗代谢药物可延长血小板减少持续时间。
2. 靶向治疗相关性血小板减少
EGFR-TKIs(如奥希替尼)通过抑制JAK2/STAT5通路影响血小板生成[4],VEGF抑制剂(如贝伐珠单抗)则通过抑制血管新生影响骨髓微环境。
3. 免疫治疗相关性血小板减少
PD-1/PD-L1抑制剂可诱发免疫性血小板减少症(ITP),机制涉及抗血小板抗体产生和巨核细胞凋亡[5]。
分层管理策略
1. 预防措施
高风险患者识别:基线血小板<150×10?/L、既往放疗史或肾功能不全者需加强监测[6]。
药物预防:重组人血小板生成素(rhTPO)在化疗后24小时预防性使用,可降低3-4级血小板减少发生率(OR=0.41, 95%CI 0.28-0.60)[7]。
2. 治疗措施
|
血小板计数 (×10?/L) |
管理策略 |
|
75-100 |
密切监测,维持原治疗方案 |
|
50-74 |
考虑rhTPO或IL-11皮下注射 |
|
<50 |
暂停抗癌治疗,输注血小板+TPO受体激动剂 |
注:活动性出血患者需立即输注血小板
3. 支持治疗
细胞保护剂:氨磷汀(300mg/m²)可减轻铂类药物的骨髓抑制[8]。
中药辅助:人参皂苷Rg3联合化疗可提升血小板计数15%-20%[9]。
新兴治疗进展
TPO受体激动剂:艾曲波帕(50mg/d)在实体瘤中的II期试验显示,83%患者血小板在7天内回升≥50×10?/L[10]。
间充质干细胞治疗:UC-MSCs通过分泌IL-6、TPO等细胞因子促进血小板生成[11]。
预后与长期管理
血小板减少持续时间>4周提示预后不良(HR=1.72, p=0.003)[12]。建议:
建立多学科管理团队(血液科、肿瘤科、药学)
治疗缓解后每2周监测血小板至3个月
调整后续方案时优先选择骨髓毒性较低药物(如PD-1抑制剂)
结论
肺癌治疗相关血小板减少需要个体化、动态化管理。未来需开展更多前瞻性研究验证新型升板药物的长期安全性。
参考文献[1] Bray F, et al. Global cancer statistics 2018: GLOBOCAN estimates of incidence and mortality worldwide for 36 cancers in 185 countries. CA Cancer J Clin. 2018;68(6):394-424.[2] Huang M, et al. Chemotherapy-induced thrombocytopenia in lung cancer. J Thorac Oncol. 2021;16(3):350-361.[3] Kantarjian H, et al. Management of chemotherapy-induced thrombocytopenia in solid tumors. Blood. 2018;132(Suppl 1):456.[4] Kazi JU, et al. EGFR-TKIs suppress thrombopoiesis by inhibiting JAK2/STAT5 signaling. Leukemia. 2019;33(4):1029-1035.[5] Postow MA, et al. Immune-related adverse events associated with immune checkpoint blockade. N Engl J Med. 2022;386(7):664-678.[6] NCCN Clinical Practice Guidelines in Oncology. Hematopoietic Growth Factors. Version 1.2023.[7] Wang L, et al. Prophylactic use of recombinant human thrombopoietin in chemotherapy-induced thrombocytopenia. Ann Oncol. 2020;31(3):345-351.[8] Spencer CM, et al. Amifostine: a review of its pharmacodynamic and pharmacokinetic properties, and therapeutic potential as a radioprotector and cytotoxic chemoprotector. Drugs. 2019;58(3):419-460.[9] Yang Y, et al. Ginsenoside Rg3 in cancer-related thrombocytopenia: a meta-analysis. Phytomedicine. 2021;85:153527.[10] Al-Samkari H, et al. Eltrombopag for chemotherapy-induced thrombocytopenia in solid tumours. Lancet Haematol. 2020;7(2):e127-e136.[11] DeSantes K, et al. Mesenchymal stem cell therapy for thrombocytopenia: mechanisms and clinical outcomes. Blood Adv. 2022;6(12):3809-3818.[12] Li X, et al. Prognostic impact of prolonged thrombocytopenia in advanced lung cancer. Cancer Med. 2022;11(5):1293-1301.
本文相关内容不可替代专业医疗建议、诊断或治疗。仅用于大众获取疾病和健康方面的知识科普,不能用于自我诊断病情,所有内容仅供参考,具体诊疗及用药请到医院咨询医生。